درمان سرطان
امروزه می توان بسیاری از سرطان ها را بیش از گذشته با موفقیت درمان کرد. امیدواری و احتمال علاج کامل یا افزایش طول عمر، هر روز بیشتر می شود که علت آن رشد آگاهی و درک ما از سرطان است. نتیجه اینکه، درمان های جدیدی که به طور گزینشی سلول های سرطانی را از بین می برند روز به روز تکامل بیشتری پیدا می کنند. چنین درمان هایی نه تنها مؤثرتر بلکه بی خطرتر هم هستند. به علاوه، کنترل درد سرطان تا نقطه ای پیشرفت کرده است که اکثر مبتلایان به سرطان قادرند همزمان با دریافت درمان ضد سرطان به زندگی روزمره ادامه داده و بدون هیچ مشکلی کار کنند.رژیم های درمانی ضد سرطان بسته به نیازهای فرد در حال درمان و نوع سرطان تنظیم می شوند. امّا، پایه و اساس همۀ گزینه های درمانی موجود برای اکثر بیماران سرطانی یکسان است. اینکه چرا یک نوع درمان مناسب تر از دیگری است به عوامل مختلفی از جمله: تشخیص، مرحله بیماری، سن، جنس و سلامت عمومی فرد بستگی دارد. در زنان، وضعیت یائسگی هم می تواند عاملی در تصمیم گیری درمان باشد.در خلال فاز تشخیص بیماری، پزشک شما معمولاً قادر به تعیین تصمیم گیری راجع به این موضوع هست که آیا برای مداوای سرطان به یک درمان موضعی مثل جراح یا تشعشع نیاز است یا به یک درمان فراگیر (سیستمیک)، مثل شیمی درمانی، به دلیل انتشار سلول های سرطانی به سایر نقاط بدن.
جراحی
جراحی، از سال ها قبل، اساس درمان سرطان بوده است. هدف از انجام هر عمل جراحی ممکن است با دیگری متفاوت باشد- گاهی برای تعیین بدخیم بودن یا نبودن یک توده، و برداشتن غده سرطانی از بدن و گاهی هم برای اطلاع از گسترش و دست اندازی سلول ها ی سرطانی به نقاط دیگر بدن انجام می شود. گاهی اوقات، جراحی اساساً به قصد باز کردن یک انسداد صورت می گیرد، مثلاً برداشتن غده ای که مجاری صفراوی را مسدود کرده است.در مواردی هم، وقتی امکان برداشت کل تودۀ سرطانی وجود ندارد، جراح تا حد امکان آن را بر می دارد (عمل توده زدایی) تا شیمی درمانی یا پرتو درمانی بر روی آن مؤثرتر انجام گیرد.جراحی، زمانی بیشترین موفقیت را دارد که سرطان در یک مکان محدود و محصور باشد (سرطان لوکالیزه یا موضعی). گاهی اوقات، امّا، سلول های سرطانی از زادگاه سرطان (محل تومور اولیه)، از طریق جریان خون یا سیستم لنفی به دیگر نقاط بدن کوچ می کنند و در آنجا تومور ثانویه ای را تشکیل می دهند (متاستاز یا دست اندازی).چنانچه سلول های سرطانی پی ش از برداشت تومور اولیه در بدن منتشر شوند، امکان ظهور مجدد سرطان در دیگر نقاط بدن حتی با وجود برداشت کامل و موفقیت آمیز تومور اولیه وجود خواهد داشت.تومور متاستاتیک (غده های دست انداخته) را باز هم براساس محل اولیه سرطان نام گذاری می کنند. مثلاً، سرطان پستان که به ریه ها گسترش پیدا کرده را دست اندازی یا متاستاز سرطان پستان می نامند، نه سرطان ریه.در صورت گسترش سرطان، با عمل جراحی به ندرت می تواند آن را علاج کرد. گهگاه پس از برداشت برداشت سرطان اولیه یک تومور منفرد متاستاتیک ظاهر می شود و در مواردی هم، برداشت یک ضایعه مفرد با عمل جراحی بهبود کامل فرد را در پی خواهد داشت. این وضعیت از جمله در مبتلایان به سرطان روده بزرگ یا بیضه ها قابل مشاهده است. دست اندازی های سرطانی (تومورهای متاستاتیک) در اکثر موارد در ریه، کبد، یا مغز اتفاق می افتند.
پرتو درمانی
تشعشع گزینۀ دیگر برای نابودسازی سلول های سرطانی است. پرتو درمانی- که گاهی به آن اشعه درمانی، درمان با اشعه ایکس یا درمان با کبالت هم می گویند- ممکن است بخشی از یک رژیم درمانی یا به تنهایی نوعی از درمان باشد. تشعشع، تنها بر سلول های سرطانی واقع د ناحیه ای از بدن تأثیر دارد که اشعه دریافتن می کنند.از تشعشع گاهی پیش از جراحی برای جمع و مچاله شدن توده سرطانی، بعد از جراحی برای نابودی بقایای سلول های سرطانی، توأم با داروها ی ضد سرطانی یا حتی به تنهایی استفاده می شود. پرتو درمانی به وِزه در انواع معینی از سرطان های موضعی، مثل توده های بدخیم گرده های لنفی یا تارهای صوتی استفاده می شود.مانند جراحی، پرتو درمانی هم معمولاً چنانچه سلول های سرطانی در سرتاسر بدن پخش شده یا خارج از محدودۀ تابش اشعه باشند، علاج قطعی نخواهد بود. البته، حتی اگر بهبود کامل در نتیجۀ پرتو درمانی محتمل نباشد، باز هم می توان از آن استفاده کرد، زیرا با جمع و مچاله کردن غده سرطانی، باعث کاهش علایم و نشانه های حاصل از آن، مثل درد یا خونریزی خواهد شد.
 شکل ۱-۱۹٫ پرتو درمانی می تواند به شکل مؤثری، سلول های سرطانی را از بین ببرد. حین درمان، منبع اشعه به آرامی می چرخد تا تأثیر تابش اشعه بیشتر شود.
شکل ۱-۱۹٫ پرتو درمانی می تواند به شکل مؤثری، سلول های سرطانی را از بین ببرد. حین درمان، منبع اشعه به آرامی می چرخد تا تأثیر تابش اشعه بیشتر شود.به طور کلی، پرتو درمانی در مقایسه با جراحی ریشه ای، بدریختی های کمتری در ظاهر فرد ایجاد می کند، امّا با این حال ممکن است عوارض جانبی مشکل سازی مثل قرمزی و سوزش یا ضخامت پوست، اشکال در بلع، خشکی دهان، تهوع، اسهال، ریزش مو و کاهش توان جسمانی، ایجاد کند. شدت و وسعت این عوارض بستگی به محل تابش و میزان اشعه تابیده شده دارد.
شیمی درمانی
شیمی درمانی عبارت است از استفادۀ فراگیر (سیستمیک) از داروهای ضد سرطان، این داروها عموماً به صورت تزریقی یا داخل وریدی تجویز می شوند. در بخشی از انواع بدخیمی، مثل بیماری هوچکین، لوسمی و سرطان بیضه، امکان بهبودی کامل با شیمی درمانی وجود دارد حتی اگر سرطان در بدن پخش شده باشد.از شیمی درمانی بیشتر به دنبال عمل جراحی برداشت تومور استفاده می شود، حتی اگر علامت واضحی از گسترش و دست اندازی تومور وجود نداشته باشد. با این نوع درمان اصطلاحاً " شیمی درمانی الحاقی" گفته می شود. در برخی از سرطان ها به ویژه سرطان سینه یا روده بزرگ و راست روده، شیمی درمانی الحاقی نشان داده است که شانس بازگشت (عود) سرطان را کاهش می دهد و افراد مبتلا به سرطان که چنین درمانی ر ا دریافت می کنند، عموماً در مقایسه با سایر افراد سرطانی عمر طولانی تری دارند.از شیمی درمان می توان پیش از عمل جراحی به منظور جمع و جور کردن غده سرطانی و در نتیجه آسان تر ساختن و موفقیت آمیز کردن عمل نیز استفاده کرد. به این نوع درمان اصطلاحاً "شیمی درمانی نوالحاقی" گفته می شود و از آن در درمان سرطان های سر، گردن و پستان استفاده می گردد. در مواردی که سرطان علاج ناپذیر است، شیمی درمانی می تواند با برطرف ساختن نشانه ها، زندگی قابل تحمل تری را برای بیماری فراهم کند. به این درمان هم اصطلاحاً "درمان تسکینی" می گویند.در شیمی درمانی ممکن است از ترکیب چند دارو استفاده کرد. شیمی درمانی ترکیبی، مستلزم تجویز گروهی از داروهاست که در کنار هم به جنگ سلول های سرطانی می روند. عیب عمدۀ داروهای ضد سرطان آن است که اینها متأسفانه، علاوه بر سلول های سرطانی، سلول های بافت طبیعی را هم تحت تأثیر قرار می دهند.سلول های طبیعی که بیش از بقیه آسیب می بینند، آنهایی هستند که سرعت تقسیم بالایی دارند مثل سلول های موجود در مغز استخوان، سلول های پوششی دستگاه گوارش، دستگاه تناسلی و فولیکول های مو البته بعد از خاتمه درمان این سلول ها معمولاً به حالت طبیعی باز می گردند.بسته به نوع خاصی از درمان که به کار می رود، شیمی درمانی می تواند عوارض جانبی متفاوتی ایجاد کند. این عوارض عبارتند از: ریزش مو، ضایعات دهانی، مشکلات بلع، خشکی دهان، تهوع، استفراغ، اسهال، خونریزی و عفونت.مشکلات کمتر شایع هم شامل: آسیب به قلب؛ کبد، ریه ها، کلیه ها، یا اعصاب می باشند. آسیب عضوی به طور معمول، خواب رفتگی یا مورمور شدن دست ها یا پاها را به دنبال دارد. در اکثر موارد، این عوارض با خاتمه درمان برطرف می شوند. متخصصان در حال پیدا کردن راهی برای کاهش یا حتی از بین بردن این اثرات جانبی هستند.
ایمنی درمانی
سیستم ایمنی بدن شما، به عنوان یک سیستم حراستی برای مقابله با آنچه از سوی او بیگانه تعبیر می شود، عمل می کند. مثلاً، موقعی که سیستم ایمنی، باکتری ها یا ویروس مضری را در بدن شما شناسایی می کند، پاسخ خود را با تولید پروتئین های ویژه ای (آنتی بادی) که به مهاجم، حمله کرده آن را نابود می سازند، نشان می دهد.سیستم ایمنی شما، سلول های سرطانی را هم به چشم مهاجمان بیگانه می نگرد. امّا به دلیل نارسایی در این سیستم، اغلب قادر به شناسایی این سلول ها نیست.سال هاست که دانشمندان در جستجوی راهی برای افزایش واکنش طبیعی سیستم ایمنی بدن به سلول های سرطانی هستند.استفاده از سیستم ایمنی برای حماسه و نابودی سلول های سرطانی را اصطلاحاً ایمنی درمانی می نامند. دیگر نام های این تکنیک عبارتند از: درمان بیولوژیک زیست درمانی (بیوتراپی) یا درمان با تعدیل پاسخ بیولوژیک. ایمنی درمانی ممکن است به تنهایی یا توأم با سایر درمان های ضد سرطان تجویز شود.یکی از شیوه های ایمنی درمانی، در واقع تجویز مواردی است که سیستم ایمنی را تحریک می کنند- ترکیبات غیر اختصاصی تعدیل کننده ایمنی. دو تا از چنین ترکیبالتی، توأم با جراحی برای سرطان مثانه و جراحی برای سرطان پیش رفته روده بزرگ مورد استفاده قرار می گیرند.روش دیگر ایمنی درمانی عبارت است از: تولید پروتئین نای اختصاصی سیستم ایمنی (سیتوکین ها) در آزمایشگاه و سپس استفاده از آنها در درمان سرطان. این پروتئین ها- که اصطلاحاً تعدیل کنده های پاسخ زیست شناختی بدن (BRMs) نامیده می شوند- بخش عمدۀ ترکیبات ایمنی درمانی را که فعلاً مورد استفاده یا مطالعه قرار می گیرند، تشکیل می دهند. بی- آر- ام ها (BRMs)
[1] عبارتند از:
اینترفرون ها
اینترفرون ها، سیتوکین هایی هستند که به طور طبیعی در بدن وجود دارند. چندین نوع انترفرون وجود دارد، امّا مورد استفاده ترین آنها در درمان سرطان، اینترفرون آلفا نام دارد. اینترفرون ها ممکن است مستقیماً سلول های سرطانی را مهار کنند یا سایر سلول های سیستم ایمنی را به نبرد با این سلول ها های سرطانی برانگیزند.از اینترفرون ها در درمان شماری از بیماری ها، از جمله: لوسمی سلول مربعی شکل، ملانوم، لوسمی میلوئید مزمن و سارکوم کاپوزی مرتبط یا ایدز استفاده می شود. همچنین مطالعاتی بر روی آنها در زمینۀ کاربرد احتمالی در درمان سرطان دست اندازی شده (متاستاتیک) کلیه و لنفوم غیر هوچکین، در حال انجام است.
اینترلوکین ها
مانند اینترفرون ها، اینترلوکین ها هم نوعی سیتوکین هستند. اینترلوکین- ۲ که بیش از بقیه اینترلوکین ها مورد مطالعه قرار گرفته، با تحریک سلول سیستم ایمنی می تواند سلول های سرطانی را نابود سازد. استفاده از آن در درمان سرطان متاستاتیک کلیه و ملانوم متاستاتیک مورد تأیید قرار گرفته، و هم اکنون برای درمان چندین سرطان دیگر تحت مطالعه است.
عوامل محرک کلونی
فاکتورها یا عوامل محرک کلونی، به جای تأثیر مستقیم بر سلول های سرطانی، باعث تولید گلبول های سفید می شوند. شیمی درمانی معمولاً عملکرد مغز استخوان از جمله: تولید گلبول های سفید، پلاکت ها و گلبول های قرمز را هم مختل می سازد.کاهش شمار این سلول ها شما را در برابر عفونت ها آسیب پذیر می سازد. CSFها یا عوامل محرک کلونی می توانند علاوه بر قابل تحمل ساختن شیمی درمانی، احتمال ایجاد عفونت و خستگی ناشی از کم خونی را که از جمله عوارض شیمی درمانی است در شما کاهش دهند.
آنتی بادی های مونوکلونال
آنتی بادی های مونوکلونال به قصد درمان انواع معینی از سرطان در آزمایشگاه طراحی و ساخته شده اند. اینها با اتصال به سلول های سرطانی، یا مستقیماً واکنش نشان می دهند یا ممکن است از آنها در ارایه داروهای ضد سرطانی یا تشعشع استفاده شود.سازمان غذا و دارو، دو تا از انواع آنتی بادی های مونوکلونال را- ریتوکسی ماب (ریتوکسان)، برای درمان لنفوم عود کننده و غیر هوچکینی سلول B، و تراستوزوماب (هرسیتین)، برای استفاده علیه سرطان متاستاتیک پستان که به شکل افراطی پروتئینی موسوم به هر- تو (اچ- ای- آر- ۲)
[۲] تولید می کند- مورد تأیید قرار داده است. آنتی بادی های مونوکلونال دیگری هم برای استفاده از انواع دیگر سرطان در حال تکوین و مطالعه هستند. این سرطان ها عبارتند از: سایر لنفوم ها، لوسمی ها، تومورهای مغزی، همین طور سرطان های ریه، روده بزرگ، راست روده و پروستات.
واکسن ها
محققان بر روی واکسن هایی کار می کنند که به سیستم ایمنی شما در شناسایی سلول های سرطانی کمک می کنند. برخلاف واکسن های مربوط به بیماری های عفونی، که برای پیشگیری از ابتلا به بیماری تجویز می شوند واکسن های سرطانی تنها بعد از ایجاد سرطان، مورد استفاده قرار می گیرند. هدف از این واکسن ها کمک به دفع تومور توسط بدن و جلوگیری از شیوع سرطان است.
عوارض جانبی
عوارض جانبی بی- آر- ام ها (BRMs) ممکن است شامل: بثورات جلدی یا ایجاد ورم در محل تزریق، نشانه های شبه آنفلوآنزایی و خستگی باشند. عوامل محرک کلونی یا سی- اس- اف ها (CSFs) ممکن است باعث درد استخوانی، خستگی، تب و بی اشتهایی شوند. دردهای مبهم استخوان و تب هم ممکن است در پی استفاده از واکسن های ضد سرطان ایجاد شوند.برخی از بی- آر- ام ها ممکنه است منجر به واکنش های حساسیتی شوند. اثرات جانبی ممکن است در مواردی شدید مشاهده شوند، لذا مشورت کردن با پزشک در مورد هر گونه اثرات جانبی احتمالی ناشی از درمان ضد سرطانی مورد استفاده در شما همیشه حائز اهمیت است.هر چه آگاهی محققان در مورد چگونگی شناسایی و حمله به سلول های سرطانی توسط سیستم ایمنی افزایش می یابد. امیدواری در زمینۀ کشف شیوه های ایمنی درمانی مؤثر علیه بسیاری از انواع سرطان هم بیشتر می شود.
حرارت درمانی
حرارت درمانی، مستلزم مواجهه ساختن بافت های بدن با حرارت های بالا- تا F· ۱۰۶ (۱/۴۱ درجه سانتی گراد)- است، حاصل ان صدمه زدن به برخی از تومورها با آسیب رساندن به سلول های بدخیم یا محروم ساختن آنها از مواد مغزی می باشد. از این نوع درمان می توان در یک بخش کوچک از بدن، مثلاً روی یک اندام یا عضو یا روی کل بدن در صورت وجود دست اندازی استفاده کرد. این درمان ممکن است باعث آزار و اذیت فرد شود و در صورت استعمال مستقیم بر روی پوست ممکن است منجر به تاول هایی گردد هر چند این تاول ها عموماً به سرعت برطرف می شوند.محققان استفاده همزمان از هیپرترمی (حرارات درمانی) در کنار شیمی درمانی و پرتودرمانی برای مداوای سرطان پستان، گره ای لنفی پوست، چشم و گردن رحم را مورد ارزیابی قرار داده اند. نقش ان همچنان در حال تحقیق و بررسی است.
سرما درمانی
سرما درمانی نقطۀ مقابل حرارت درمانی است. در اینجا برای نابودی سلول های سرطانی از سرمای بسیار شدید استفاده می شود. سرما درمانی استعمال نیتروژن مایع به داخل تومور است. از آن بیشتر برای درمان سرطان های پوست در مراحل اولیه و بیماری های پیش سرطانی پوست، همین طور سرطان شبکیه (رتینوبلاستوم) استفاده می شود. محققان در حال مطالعه بر روی سرما درمانی به عنوان یک درمان محتمل برای برخی از سرطان های داخلی مثل سرطان پروستات و کبد، هستند. در این سرطان ها، نیتروژن مایع را از طریق ابزاری موسوم به کرایوپروب (سرمابر) به تومور می رسانند.
پیوند سلول بنیادی
از پیوند سلول بنیادی در جایگزین ساختن سلول های داخل مغز استخوان که در نتیجۀ شیمی درمانی یا تشعشع تخریب شده است، استفاده می شود. حین عمل شما مقدار معینی از سلول های بنیادی را دریافت می کنید- سلول های نارسی که هنوز در انواع متنوع سلول های خونی تمایز نیافته اند. شما ممکن است سلول های بنیادی را از خودتان (پیوند خودزاد)
[۳]، یا از یک دو قلوی همسان، در صورتی که دوقلو باشید (پیوند همزاد)
[۴]، یا از یک خواهر یا برادر یا یکی از والدین یا حتی یک دهنده غریبه (پیوند ناهمزاد)
[۵]، دریافت کنید. آگاهی از این موضوع که شما ذخیره کافی و در دسترسی از سلول های بنیادی سالم دارید، به پزشکتان این اجازه را می دهد تا از دوزهای بالای شیمی درمانی یا تشعشع استفاده کند. از پیوند سلول بنیادی بیشتر برای درمان لوسمی و لنفوم استفاده می شود.
مهار کننده های رگ سازی
همه تومورها برای رساندن اکسیژن و مواد مغزی به سلول های خود برای رشد آنها به عروق خونی جدید نیاز دارند. تشکیل عروق خونی جدید را اصطلاحاً آنژیوژنز یا "رگ سازی" می نامند. دانشمندان در حال مطالعه بر روی استفاده از هر نوع مهارکننده طبیعی و مصنوعی رگ سازی، برای جمع و کوچک شدن تومورها یا جلوگیری از رشد آنها با ممانعت از تشکیل عروق خونی جدید هستند.
درمان های نوظهور
درمان سرطان دائماً در حال تحول است. برخی از روش هایی که در اینجا ذکر شده اند، در حال حاضر به عنوان یک شیوه درمان مورد تأیید قرار گرفته اند و برخی هنوز تحت تحقیق و بررسی قرار داشته و درمان های آزمایشگاهی به شمار می روند. پزشکان، اغلب این رویکردها را با شیمی درمانی و پرتو درمانی تلفیق می کنند.
ژن درمانی
علت رشد و ظهور تومورها، آسیب دیدن ژن های طبیعی است که باعث می گردد سلول های سالم، سرطانی شوند. ژن هایی که سرکوبگر سرطان هستند نیز ممکن است دچار نقص عملکرد شوند. هدف از ژن درمانی، ترمیم یا جایگزینی ژن های معیوب و افزایش تولید ژن های سالم است.
درمان مولکولی
سازمان غذا و دارو استفاده از داروی ایماتینیب مسیلیت (گلیوک، اس- تی- آی- ۵۷۱)
[۶] را برای درمان لوسمی میلوئید مزمن، که نوعی سرطان نادر می باشد، مورد تأیید قرار داده است. این لوسمی ناشی از نوعی جهش ژنتیکی است که امکان روشن (فعّال) ماندن دایمی یک آنزیم مربوط به سلول های خونی را فراهم می سازد. داروی مذکور باعث مهار این آنزیم و در نتیجه ممانعت از رشد غیرطبیعی گلبول های سفید خون می شود.تراستوزوماب (هرسپتین)
[۷] درمان دیگری است که هدف آن نوعی پروتئین ویژه، موسوم به هر- تو- نوی
[۸] می باشد که توسط یک ژن معیوب ساخته می شود. این پروتئین در یکی از هر چهار بیمار مبتلا به سرطان پستان یافت می شود.هرسپتین نوعی آنتی بادی مونوکلونال است که با اتصال به پروتئین معیوب باعث کاهش رشد سلول و حتی مکرگ سلول های سرطانی می گردد. برخلاف اکثر آنتی بادی های مونوکلونال، این دارو برای تأثیر داشتن در قبال سلول های سرطانی به سیستم ایمنی وابسته نیست.
جراحی با لیزر
پرتوهای لیزر، ابزار قدرتمندی برای انجام اعمال جراحی دقیق هستند. از جراحی با لیزر غالباً درمان سرطان های پوست، ریه، تارهای صوتی، مهبل، فرج، گردن رحم و آلت مردان استفاده می شود. گرمای ساطع شده از پرتو لیزر می تواند به علاوه با جمع و کوچک ساختن تومور باعث برطرف شدن نشانه های مربوط به سرطان گردد.
نوردرمانی
در فرایند نور درمانی، سلول های سرطانی ابتدا با ترکیبات حساس کننده در برابر نور، درمان شده و سپس د معرض نور لیزر قرار می گیرند. نور لیزر جذب شده در سلول های بدخیم منجر به نوعی واکنش شیمیایی می شود که نابودی این سلول ها را در پی دارد. مزیت این نوع درمان آن است که بسیار گزینشی عمل می کند، یعنی تنها بر سلول های سرطانی عمل می کند و به سلول های طبیعی مجاور آسیبی نمی زند. در این روش از نور لیزری استفاده می شود که تنها قادر به عبور از لایۀ نازکی از بافت می باشد و از این رو بذرهای سرطان های سطحی مفید بوده و تأثیری بر سرطان های عمقی اعضاء بدن ندارد. محققان هم اکنون در حال پیدا کردن راه هایی برای ارتقاء این وجه از نور درمانی هستند.
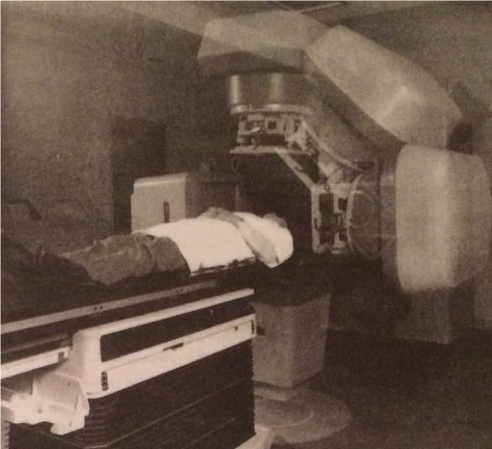 شکل ۱-۱۹٫ پرتو درمانی می تواند به شکل مؤثری، سلول های سرطانی را از بین ببرد. حین درمان، منبع اشعه به آرامی می چرخد تا تأثیر تابش اشعه بیشتر شود.به طور کلی، پرتو درمانی در مقایسه با جراحی ریشه ای، بدریختی های کمتری در ظاهر فرد ایجاد می کند، امّا با این حال ممکن است عوارض جانبی مشکل سازی مثل قرمزی و سوزش یا ضخامت پوست، اشکال در بلع، خشکی دهان، تهوع، اسهال، ریزش مو و کاهش توان جسمانی، ایجاد کند. شدت و وسعت این عوارض بستگی به محل تابش و میزان اشعه تابیده شده دارد.
شکل ۱-۱۹٫ پرتو درمانی می تواند به شکل مؤثری، سلول های سرطانی را از بین ببرد. حین درمان، منبع اشعه به آرامی می چرخد تا تأثیر تابش اشعه بیشتر شود.به طور کلی، پرتو درمانی در مقایسه با جراحی ریشه ای، بدریختی های کمتری در ظاهر فرد ایجاد می کند، امّا با این حال ممکن است عوارض جانبی مشکل سازی مثل قرمزی و سوزش یا ضخامت پوست، اشکال در بلع، خشکی دهان، تهوع، اسهال، ریزش مو و کاهش توان جسمانی، ایجاد کند. شدت و وسعت این عوارض بستگی به محل تابش و میزان اشعه تابیده شده دارد.